On teada, et kõik ained koosnevad molekulidest. Kuid millest on molekulid ise valmistatud? Vaatame seda küsimust üksikasjalikumalt.
Mis on molekul?
Nimi "molekul" pärineb ladina molekulist - see on sõna moolide (tõlgitud mass) deminutiiv. Nende olemasolu tõestas esmakordselt prantsuse füüsiku J. Perrini 1906. aastal tehtud katses, kui ta uuris Browniani liikumist.

Keemias on see eraldi aineosakese nimi, mis koosneb kahest või enamast aatomist, mis on omavahel seotud kovalentsete sidemetega. Kvantmehaanika määratleb seda süsteemina, mis koosneb mitte aatomitest, vaid nende tuumadest ja nendega interakteeruvatest elektronidest.
Huvitav fakt: Füüsika nimetab molekulideks mitte ainult polüatomilisi osakesi, vaid ka monatomseid osakesi, mis koosnevad aatomitest, mis pole ühendatud keemiliste sidemetega (puhas elavhõbe või inertgaasid). Sel juhul ühendatakse mõisted “molekul” ja “aatom”.
Tavaliselt on molekulid elektriliselt neutraalsed, kuna prootonite ja elektronide arv neis on sama, kuid on ka molekule, millel on elektrilaeng (neid nimetatakse ioonideks).
Suure molekulmassiga aine osakesi nimetatakse makromolekulideks. Need koosnevad valkudest, nukleiinhapetest, ensüümidest, polüsahhariididest, aminohapetest, keerulistest lipiididest ja üksikutest kunstlikult loodud ühenditest, näiteks polümeeridest. Nende hulka kuulub sadu ja tuhandeid aatomeid. Süsivesinike derivaadid - orgaanilised ained ja biopolümeerid, reeglina, ei oma mitte ainult suurt massi, vaid on ka keerukamad kui anorgaanilised ühendid.
Molekulaarne struktuur
Mis tahes ühendi molekulil on sama koostis, sellel on alati sama arv aatomeid, keemilised omadused sõltuvad valentssidemetest, mis neid koos hoiavad. Klassikalises teoorias peetakse molekuli dünaamiliseks struktuuriks, mis koosneb aatomituumadest ja nende rühmadest ning teatud arvust elektronidest, mis paiknevad sisemisel ja välimisel tasandil.
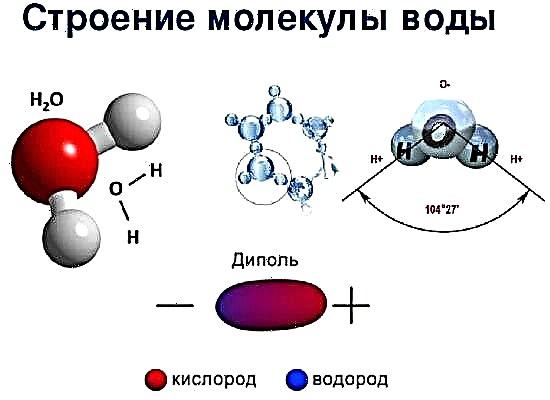
Keemilised sidemed moodustavad tavaliselt ainult väliseid elektrone. Sideme loovad 1,2 või 3 paari elektrienergiat kahest naaberaatomist (mille tulemusel ilmub elektronpilv). Aatomite interaktsioonienergia sõltub nende asukohast ja see aitab molekuli stabiilsusele tavalistes tingimustes: see ei võimalda aatomitel liiga lähestikku pääseda.
Aatomeid saab laadida positiivselt ja negatiivselt, nende arv on alati konstantne. Teatud aine molekulide struktuuri ja koostist ei mõjuta selle saamise viis, see tähendab, et kunstlikult toodetud aine on täpselt samasugune kui looduslik.
Molekulaarne koostis kirjutatakse keemiliste valemite abil. Struktuur määrab, millised füüsikalised omadused ainel on.
Huvitav fakt: orgaaniline aine, vesi, süsinikdioksiid sulavad ja keevad suhteliselt madalatel temperatuuridel ning säilitavad nende struktuuri tahkes olekus. Paljud anorgaanilised ained ei koosne molekulidest, vaid aatomitest (kristallid, puhtad metallid jne).
Molekulid teaduses
Keemias on see põhikontseptsioon, molekulide struktuur määratakse keemiliste reaktsioonide alusel ainega.Samuti on struktuuri teades võimalik kindlaks teha, millised on reaktsioonid. Keemiliste uuringute tulemusel saadi suurem osa teadmisi molekulaarse funktsionaalsuse ja struktuuri kohta.
Füüsika struktuur selgitab vedelike, gaaside ja tahkete ainete füüsikalisi omadusi. Molekulide liikuvus määrab, kui kiiresti aine suudab kokkupuutel teise tungida, viskoossuse taseme ja soojusjuhtivuse määra.
Bioloogias on molekulaarsed omadused ja ruumiline struktuur ülimalt tähtis, kuna kõik elusolendid toimivad molekulide (keemiliste ja mittekeemiliste) vastastikmõjude tundliku tasakaalu tõttu.
Küsimusele, mis molekulid koosnevad, saab vastata nii - teatud hulgast aatomitest, mis on ühendatud keemiliste sidemetega. Kõik planeedi ained koosnevad molekulidest.mille füüsikalised ja keemilised omadused on määratud molekulide struktuuri ja koostisega.